系统分析总结化学催化反应的特点,并说明为什么可逆反应的催化剂在加快正反应的同时也将同样加快逆反应?
正确答案:
(1)化学催化反应的特点:
①催化剂本身在反应前后不发生变化,催化剂能够反复利用,所以一般情况下催化剂的用量很少。
②催化剂只能改变反应的历程和反应速率,不能改变反应的产物。
③对于可逆反应,催化剂不改变反应的平衡状态,即不改变化学平衡关系。
④催化剂对反应有较好的选择性,一种催化剂一般只能催化特定的一个或一类反应。
(2)催化剂能加快逆反应的原因如下:
可逆反应的化学平衡常数(K)与反应的自由焓变化(ΔG0)有ΔG0=-RTlnK
即K决定于ΔG0,无论有没有催化剂的存在,ΔG0不变,因此K也不变。
对于A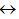 P的可逆反应,K与正、负反应的反应速率常数k1和k2有K=k1/k2
P的可逆反应,K与正、负反应的反应速率常数k1和k2有K=k1/k2
又由于K值不变,所以催化剂在加快正反应的同时,也必将加快逆反应。
①催化剂本身在反应前后不发生变化,催化剂能够反复利用,所以一般情况下催化剂的用量很少。
②催化剂只能改变反应的历程和反应速率,不能改变反应的产物。
③对于可逆反应,催化剂不改变反应的平衡状态,即不改变化学平衡关系。
④催化剂对反应有较好的选择性,一种催化剂一般只能催化特定的一个或一类反应。
(2)催化剂能加快逆反应的原因如下:
可逆反应的化学平衡常数(K)与反应的自由焓变化(ΔG0)有ΔG0=-RTlnK
即K决定于ΔG0,无论有没有催化剂的存在,ΔG0不变,因此K也不变。
对于A
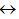 P的可逆反应,K与正、负反应的反应速率常数k1和k2有K=k1/k2
P的可逆反应,K与正、负反应的反应速率常数k1和k2有K=k1/k2又由于K值不变,所以催化剂在加快正反应的同时,也必将加快逆反应。
答案解析:有

微信扫一扫手机做题
